Le virus d’Epstein-Barr (EBV) est présent dans 95% de la population mondiale. Chez les personnes infectées, des anticorps anti-EBV circulent pendant toute leur vie. Des chercheurs et chercheuses de l’Inserm (Institut national de la santé et de la recherche médicale), d’Université de Paris, de Sorbonne Université et du CNRS (Centre national de la recherche scientifique) ont eu l’idée de réorienter cette réponse immunitaire contre des cellules cibles prédéfinies en fonction d’une maladie à soigner.
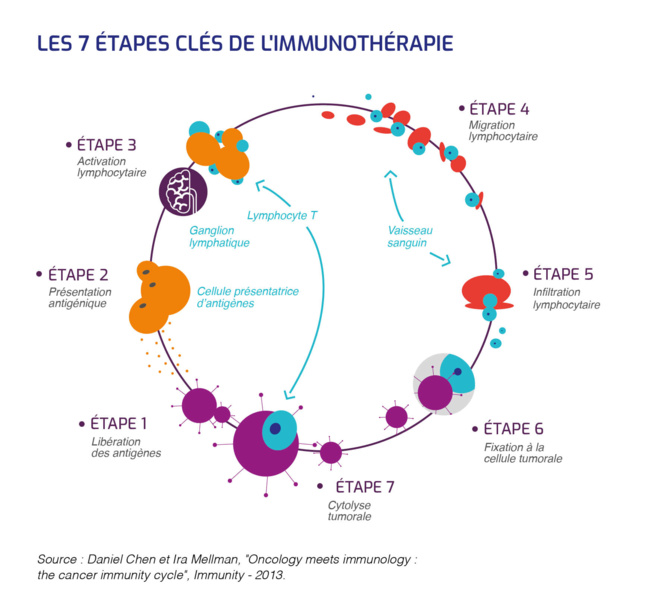
Pour cela, ils ont conçu des protéines dites de fusion bi-modulaires (BFMPs) : elles comportent un domaine qui se fixe spécifiquement à un antigène de surface de la cellule que l’on cherche à détruire. Ce domaine est lié à l’antigène EBV-P18 de l’EBV, contre lequel des anticorps (IgG) sont déjà présents dans l’organisme du patient. Les cellules cibles sont traitées avec les BFMPs spécifiques, ce qui induit le recrutement des IgG anti-EBV-P18 et l’activation des défenses immunitaires, avec in fine la destruction de ces cellules-cibles.
Le procédé a d’abord été testé in vitro, puis dans un modèle animal de cancer, aboutissant à une augmentation significative de la survie, voire à la rémission totale du cancer chez certains animaux. Le travail de l’équipe a été publié dans Science Advances.
Pour cela, ils ont conçu des protéines dites de fusion bi-modulaires (BFMPs) : elles comportent un domaine qui se fixe spécifiquement à un antigène de surface de la cellule que l’on cherche à détruire. Ce domaine est lié à l’antigène EBV-P18 de l’EBV, contre lequel des anticorps (IgG) sont déjà présents dans l’organisme du patient. Les cellules cibles sont traitées avec les BFMPs spécifiques, ce qui induit le recrutement des IgG anti-EBV-P18 et l’activation des défenses immunitaires, avec in fine la destruction de ces cellules-cibles.
Le procédé a d’abord été testé in vitro, puis dans un modèle animal de cancer, aboutissant à une augmentation significative de la survie, voire à la rémission totale du cancer chez certains animaux. Le travail de l’équipe a été publié dans Science Advances.